糖尿病足是糖尿病最严重的慢性并发症之一,其高致残率与高死亡率严重威胁患者生活质量。本文系统阐述了糖尿病足的多因素形成原因,深入分析了其难以愈合的核心机制,探讨了黄芪多糖促进伤口愈合的药理作用,并总结了有助于加速伤口愈合的饮食策略。研究表明,糖尿病足的发生与神经病变、血管病变、感染等多因素相互作用密切相关;难愈性主要源于高血糖微环境、免疫功能障碍、组织修复异常及持续感染等病理过程;黄芪多糖可通过抗炎、促血管生成、调节免疫等多途径促进创面修复;合理的饮食干预(如高蛋白、维生素C/E、锌等营养素补充)能为伤口愈合提供物质基础。本文为糖尿病足的预防与治疗提供了理论参考。
糖尿病足(Diabetic Foot Ulcer, DFU)是指糖尿病患者因下肢远端神经异常和不同程度的周围血管病变导致的足部感染、溃疡和(或)深层组织破坏,是糖尿病最复杂的并发症之一。据统计,全球约15%~25%的糖尿病患者一生中会发展为糖尿病足,其中14%~24%的患者最终面临截肢风险,截肢后5年死亡率高达40%~70%。糖尿病足的治疗难点在于其“难愈合性”,传统治疗手段(如清创、抗感染、改善循环)效果有限,亟需从病因机制及新型干预策略(如中药活性成分、营养支持)层面探索突破。本文结合国内外研究进展,系统解析糖尿病足的形成原因、难愈机制,并重点探讨黄芪多糖的药理作用及饮食干预策略。
一、糖尿病足的形成原因
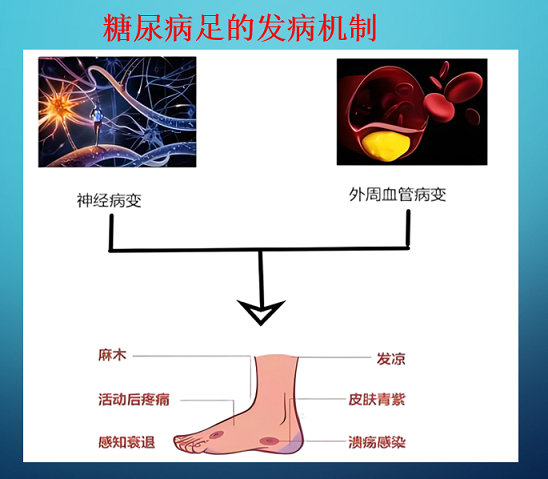
糖尿病足的发生是多因素协同作用的结果,主要包括神经病变、血管病变、感染及足部机械应力异常四大核心环节。
(一)神经病变:感觉与运动功能丧失的基础
糖尿病周围神经病变(Diabetic Peripheral Neuropathy, DPN)是糖尿病足的首要危险因素,约60%~70%的糖尿病足患者合并DPN。长期高血糖通过多元醇通路激活、蛋白激酶C(PKC)通路异常、晚期糖基化终末产物(AGEs)积累等机制,损伤周围神经轴索及髓鞘,导致感觉神经、运动神经及自主神经功能障碍。
感觉神经受损:患者足部痛觉、触觉、温度觉减退或消失,无法感知外伤(如鞋磨破、烫伤、异物刺伤),形成“无痛性溃疡”;
运动神经受损:足部小肌肉萎缩(如趾间肌、骨间肌),导致足弓塌陷、爪形趾畸形,足底压力分布异常,局部组织长期受压缺血;
自主神经受损:足部汗腺分泌减少,皮肤干燥皲裂,屏障功能下降,易继发细菌感染。
(二)血管病变:组织缺血缺氧的关键
糖尿病周围血管病变(Diabetic Peripheral Vascular Disease, PVD)是糖尿病足进展的重要推手,主要表现为下肢动脉粥样硬化及微循环障碍。高血糖通过氧化应激、炎症反应损伤血管内皮细胞,促进平滑肌细胞增殖及脂质沉积,导致动脉管腔狭窄甚至闭塞;同时,毛细血管基底膜增厚、内皮细胞间隙增大,红细胞变形能力下降,微循环灌注不足。缺血状态下,足部组织氧分压降低,代谢废物堆积,不仅直接抑制细胞增殖与胶原合成,还会加重神经病变,形成“神经-血管恶性循环”。
(三)感染:溃疡恶化的催化剂
糖尿病患者免疫力低下(如中性粒细胞趋化、吞噬功能减弱,淋巴细胞增殖反应受损),且足部皮肤破损后,细菌(如金黄色葡萄球菌、大肠杆菌、厌氧菌)易侵入皮下组织。高糖环境为细菌提供了丰富的碳源,同时AGEs可增强细菌生物膜形成能力,导致感染迁延不愈。感染进一步加重局部炎症,释放大量基质金属蛋白酶(MMPs),降解细胞外基质,扩大溃疡面积,甚至引发骨髓炎、脓毒血症。
(四)足部机械应力异常:溃疡发生的始动因素
除神经、血管病变外,足部生物力学异常是溃疡形成的直接诱因。长期高血糖导致足部关节活动受限、肌腱纤维化,足底压力向跖骨头、足跟等部位集中,形成“压力性溃疡”。此外,不合适的鞋袜、修剪趾甲不当、外伤等外部因素,在神经感觉缺失的情况下,极易诱发皮肤破损,进而发展为糖尿病足。
二、糖尿病足难以愈合的机制
糖尿病足的“难愈性”是其病理生理特点的综合体现,核心机制可归纳为以下四方面:
(一)高血糖微环境的毒性作用
持续高血糖通过多种途径抑制伤口愈合:① AGEs蓄积:葡萄糖与蛋白质非酶促反应生成AGEs,其与受体(RAGE)结合后激活NF-κB通路,促进TNF-α、IL-6等促炎因子释放,加重局部炎症;② 氧化应激失衡:线粒体电子传递链在高糖状态下产生过量活性氧(ROS),超出抗氧化系统清除能力,导致细胞DNA、蛋白质及脂质损伤,抑制成纤维细胞增殖与迁移;③ 代谢紊乱:高血糖抑制己糖激酶活性,减少ATP生成,同时激活多元醇通路,消耗NADPH,削弱谷胱甘肽还原酶活性,进一步加剧氧化应激。
(二)免疫功能紊乱:炎症失控与修复受阻
糖尿病状态下,固有免疫与适应性免疫功能均受损:① 中性粒细胞功能障碍:趋化因子(如CXCL8)表达降低,中性粒细胞无法有效募集至创面,吞噬杀菌能力下降;② 巨噬细胞极化异常:M1型巨噬细胞(促炎)比例升高,M2型(抗炎、促修复)比例降低,导致炎症期延长,无法进入增殖期;③ T细胞应答减弱:Th1/Th2平衡失调,IL-2、IFN-γ等细胞因子分泌减少,影响细胞免疫及胶原合成。
(三)组织修复细胞功能抑制
伤口愈合依赖成纤维细胞、内皮细胞、角质形成细胞的增殖与分化,而糖尿病微环境显著抑制其功能:① 成纤维细胞:高糖环境下,TGF-β/Smad通路受阻,α-SMA(肌成纤维细胞标志物)表达降低,胶原(Ⅰ、Ⅲ型)合成减少,且MMPs/TIMPs(基质金属蛋白酶/抑制剂)失衡,导致细胞外基质降解大于合成;② 内皮细胞:VEGF(血管内皮生长因子)表达下调,血管新生受阻,创面血供难以恢复;③ 角质形成细胞:迁移能力减弱,上皮化延迟,创面长期暴露易继发感染。
(四)持续感染与生物膜形成
如前所述,糖尿病足溃疡常合并细菌感染,且细菌易形成生物膜(由胞外聚合物EPS包裹的细菌群落)。生物膜可抵抗抗生素渗透,降低免疫细胞杀伤效率,导致感染反复发作。此外,细菌代谢产物(如短链脂肪酸、内毒素)进一步破坏创面微环境,抑制肉芽组织生长。
三、黄芪多糖对伤口愈合的作用
黄芪多糖(Astragalus Polysaccharides, APS)是从豆科植物蒙古黄芪或膜荚黄芪根中提取的水溶性杂多糖,具有免疫调节、抗炎、抗氧化、促血管生成等多种药理活性,近年来被广泛研究用于促进糖尿病足等慢性创面愈合。
(一)抗炎作用:调控炎症因子网络
黄芪多糖可通过抑制NF-κB通路减轻创面过度炎症:一方面,减少TNF-α、IL-6、IL-1β等促炎因子的mRNA表达;另一方面,促进IL-10(抗炎因子)释放,加速炎症期向增殖期转化。研究发现,糖尿病大鼠创面局部应用APS后,M1型巨噬细胞浸润减少50%,M2型比例升高2倍,炎症持续时间缩短3~5天。
(二)促血管生成:改善局部血供
黄芪多糖能促进内皮细胞增殖、迁移及管腔形成,其机制与上调VEGF、bFGF(碱性成纤维细胞生长因子)表达有关。体外实验显示,黄芪多糖(100~200 μg/mL)可使人脐静脉内皮细胞(HUVECs)的VEGF mRNA表达增加3.2倍,管状结构形成数量增加4倍;动物实验中,糖尿病小鼠创面经APS处理后,微血管密度提高60%,氧分压从20 mmHg升至45 mmHg,有效缓解缺血状态。
(三)抗氧化应激:保护修复细胞
黄芪多糖可增强机体抗氧化能力:通过提高超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)活性,降低丙二醛(MDA)含量,减少ROS对成纤维细胞、角质形成细胞的损伤。在链脲佐菌素(STZ)诱导的糖尿病大鼠模型中,腹腔注射APS(200 mg/kg/d)7天后,创面组织SOD活性升高40%,MDA水平降低35%,成纤维细胞存活率从45%提升至78%。
(四)促进细胞增殖与基质合成
黄芪多糖能直接刺激成纤维细胞增殖,并促进胶原、纤连蛋白等ECM成分合成。机制研究表明,黄芪多糖可激活PI3K/Akt/mTOR通路,上调Cyclin D1(细胞周期蛋白)表达,加速成纤维细胞从G0/G1期进入S期;同时,通过TGF-β1/Smad2/3通路促进α-SMA、ColⅠ、ColⅢ表达,增强肉芽组织抗张强度。临床研究显示,糖尿病足溃疡患者局部应用黄芪多糖凝胶后,溃疡面积缩小速度较对照组快2.3倍,平均愈合时间缩短12天。
四、促进糖尿病足伤口愈合的饮食策略
饮食干预是糖尿病足治疗的基础,通过补充关键营养素,可为组织修复提供原料,改善代谢状态,增强免疫与抗氧化能力。
(一)优质蛋白质:组织修复的物质基础
蛋白质是成纤维细胞、内皮细胞增殖及胶原合成的必需原料。建议每日摄入1.2~1.5 g/kg体重的优质蛋白,来源包括:
动物蛋白:鱼(如三文鱼、鳕鱼,富含Omega-3脂肪酸,抗炎)、瘦肉(鸡胸肉、瘦牛肉,含支链氨基酸)、鸡蛋(全蛋,含生物利用率最高的蛋白质);
植物蛋白:大豆及其制品(豆腐、豆浆,含异黄酮,抗氧化)、坚果(杏仁、核桃,含锌、维生素E)。
注意:合并肾功能不全者需限制蛋白摄入量(0.8 g/kg/d),并在医生指导下调整。
(二)维生素C与维生素E:抗氧化与胶原合成的关键
维生素C:参与脯氨酸、赖氨酸羟化,促进胶原交联;同时作为抗氧化剂清除自由基。推荐每日摄入100~200 mg,来源为鲜枣、猕猴桃、青椒、草莓。
维生素E:脂溶性抗氧化剂,保护细胞膜免受ROS损伤,促进成纤维细胞迁移。建议每日摄入15~20 mg,来源为植物油(橄榄油、葵花籽油)、坚果、麦胚。
(三)锌:细胞增殖与免疫调节的必需元素
锌是DNA聚合酶、RNA聚合酶的辅酶,参与细胞分裂与蛋白质合成;同时可增强中性粒细胞趋化与吞噬功能。缺锌会导致成纤维细胞增殖抑制、溃疡愈合延迟。推荐每日摄入12~15 mg,来源为牡蛎、红肉、动物肝脏、豆类。
(四)其他有益营养素
精氨酸:通过NO/cGMP通路促进血管舒张与内皮细胞增殖,来源为海参、鳝鱼、花生;
谷氨酰胺:肠黏膜细胞与免疫细胞的主要能源物质,可增强肠道屏障功能,减少内毒素入血,来源为乳清蛋白、卷心菜、菠菜;
Omega-3脂肪酸:抑制AA(花生四烯酸)代谢,减少促炎因子(如LTB4)生成,来源为深海鱼、亚麻籽、紫苏油。
(五)饮食禁忌
严格控糖:避免精制碳水化合物(白米饭、馒头、甜点),选择低GI食物(燕麦、糙米、荞麦),维持血糖稳定(空腹<7.0 mmol/L,餐后<10.0 mmol/L);
限制饱和脂肪与反式脂肪:减少动物内脏、肥肉、油炸食品摄入,避免血脂升高加重血管病变;
戒烟限酒:烟草中的尼古丁收缩血管,酒精抑制成纤维细胞增殖,均需严格禁止。
结论
糖尿病足的形成是神经病变、血管病变、感染及机械应力异常共同作用的结果,其难愈性源于高血糖微环境的毒性作用、免疫紊乱、修复细胞功能抑制及持续感染。黄芪多糖通过抗炎、促血管生成、抗氧化及促进细胞增殖等多靶点作用,成为促进糖尿病足愈合的潜在药物;而合理的饮食干预(高蛋白、充足维生素与矿物质、控糖)则为伤口愈合提供了物质基础与代谢保障。
声明:本文来源于网络,如有侵权我们深感歉意,请联系我们,定在第一时间删除
人参黄精菊苣复合片主要成分:
灵芝粉、菊苣粉、槐米粉、黄精粉、沙棘粉、枸杞粉、黄芪粉、人参粉、绿咖啡粉、金银花粉、维生素B1、维生素B2

复合小分子肽主要成分:人参(五年以下人工种植)、牛骨髓肽、海洋鱼低聚肽、牡蛎肽、地龙蛋白肽、苦瓜肽、纳豆粉、菊粉

咨询微信:1502660026

说明:本站分享的产品是食品,不是药物,不能代替药物和医院治疗疾病!
分享内容均转自互联网,仅做参考,如您有疾病,建议您去看医生!我们理念是平时要注重养生与营养!
温馨提示:为了您的健康,克制不良的生活习惯,戒烟、限酒,不吃各种油炸食品、方便面、烧烤肉类、少吃工厂的各种加工食品,多吃新鲜蔬菜、水果,适当增加粗粮,配合服用等,详情咨询客服!
特别声明:本文来源于网络,如有侵权我们深感歉意,请联系我们,定在第一时间删除!
糖尿病足的形成原因有哪些糖尿病足怎么形成的糖尿病足怎么快速愈合糖尿病足怎么调理糖尿病足适合吃什么食物调理糖尿病足为什么难愈合黄芪多糖对伤口愈合的作用糖尿病足难以愈合的机制促进糖尿病足伤口愈合的饮食干预

